為全面反映2020年我國醫療器械不良事件監測工作情況,國家藥品不良反應監測中心編撰了《國家醫療器械不良事件監測年度報告(2020年)》。
一、醫療器械不良事件監測工作進展
2020年,我國醫療器械不良事件監測工作繼續堅持“四個最嚴”的要求,貫徹落實《醫療器械不良事件監測和再評價管理辦法》(以下簡稱《辦法》),以評價醫療器械風險為主線,以落實醫療器械注冊人和備案人(以下簡稱注冊人)不良事件監測主體責任為重點,繼續加強制度體系建設、不斷拓展宣傳培訓方式、深入探索監測評價方法、全面提升風險預警和處置能力,醫療器械不良事件監測工作取得了新的進展。
(一)推進報告收集工作、擴大系統覆蓋用戶
2020年,國家醫療器械不良事件監測信息系統接收到醫療器械不良事件報告53萬余份,每百萬人口平均報告數為402份。28個省(自治區、直轄市)的醫療器械不良事件報告縣級覆蓋率達到100%。此外,醫療器械不良事件監測系統基層注冊用戶數量持續提升,達到35萬余家,其中醫療器械注冊人達27,195家。
(二)深入挖掘產品風險、完成重點監測工作
2020年,醫療器械不良事件風險評價處置工作深入開展。強化對全國醫療器械不良事件報告的日常監測、預警分析及季度匯總,根據發現的風險情況,全年共發布《醫療器械不良事件信息通報》1期、《醫療器械警戒快訊》12期。完成“十三五”醫療器械不良事件重點監測工作任務,各承擔單位積極回顧前期工作,梳理產品風險,按要求報送重點監測品種風險評價報告和“十三五”重點監測工作總結報告。
(三)開展法律法規培訓、積極參與國際交流
2020年,國家藥品不良反應監測中心共培訓注冊人、醫療機構、監測機構人員1000余人次,同時為各級藥品監管部門、監測機構組織開展的相關培訓班提供師資,強化注冊人主體責任,提升監測人員能力水平,取得了較好的培訓效果。此外,積極跟進國際醫療器械監管機構論壇不良事件術語和編碼(AET)、患者登記(PR)兩個項目的工作進展,并積極參與國家監管機構報告(NCAR)項目工作,開展報告信息交換,國際化水平進一步提升。
二、全國醫療器械不良事件報告總體情況
(一)年度報告總體情況
1.全國醫療器械不良事件報告數量。2020年,國家醫療器械不良事件監測信息系統共收到醫療器械不良事件報告536,055份,比上年增加35.25%(圖1)。
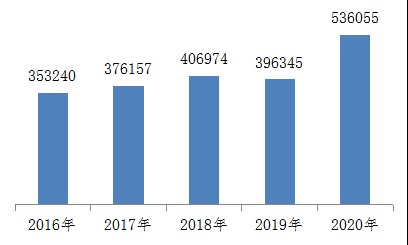
圖1 2016-2020年全國醫療器械不良事件報告數量

2.每百萬人口平均報告數量。2020年,我國每百萬人口平均醫療器械不良事件報告數為402份,比上年增加35.35%(圖2)。
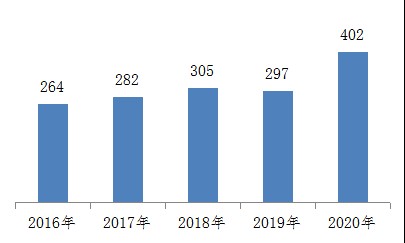
圖2 2016-2020年全國每百萬人口平均醫療器械不良事件報告數比較
(二)全國注冊基層用戶數量
截至2020年12月31日,在國家醫療器械不良事件監測信息系統中注冊的基層用戶(包括注冊人、經營企業和使用單位)共350,973家,其中注冊人27,195家,占用戶總數的7.75%;經營企業198,833家,占用戶總數的56.65%;使用單位124,945家,占用戶總數的35.60%(圖3)。
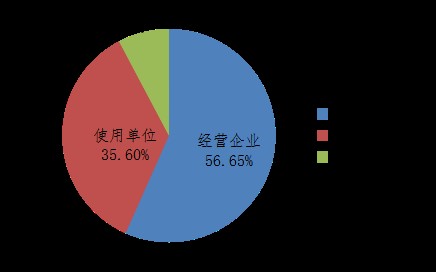
圖3 2020年國家醫療器械不良事件監測信息系統注冊基層用戶情況
2020年,注冊基層用戶總數比上年增長10.03%。其中,注冊人注冊基層用戶比上年增長38.31%,經營企業和使用單位的注冊基層用戶分別比上年增長11.52%和3.24%(圖4)。
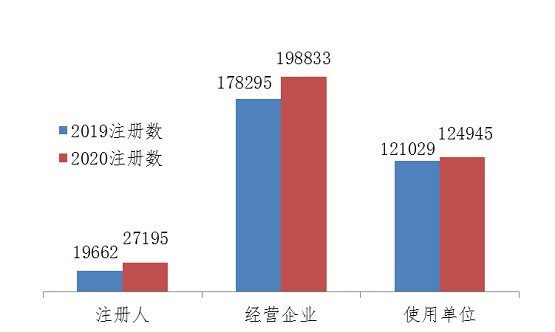
圖4 2019、2020年國家醫療器械不良事件監測信息系統注冊基層用戶分類比較情況
三、全國醫療器械不良事件報告統計分析
(一)按報告來源統計分析
2020年,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,使用單位上報455,782份,占報告總數的85.03%;注冊人上報11,191份,占報告總數的2.09%;經營企業上報68,902份,占報告總數的12.85%;其他來源的報告180份,占報告總數的0.03%(圖5)。
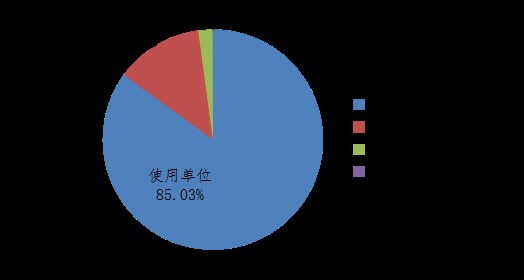
圖5 2020年醫療器械不良事件報告來源情況
(二)按事件傷害程度統計分析
2020年,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,傷害程度為死亡的報告218份,占報告總數的0.04%;傷害程度為嚴重傷害的報告32,874份,占報告總數的6.13%;傷害程度為其他的報告502,963份,占報告總數的93.83%(圖6)。
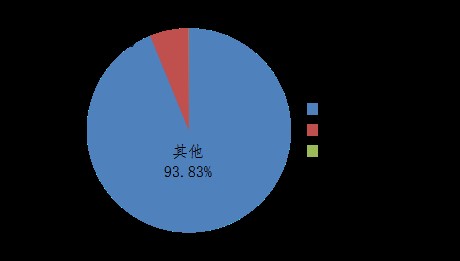
圖6 2020年醫療器械不良事件報告涉及事件傷害程度情況

2020年,對于事件傷害程度為死亡的醫療器械不良事件報告,國家藥品不良反應監測中心均及時進行了處置,督促注冊人開展調查、評價。在目前完成分析評價的事件中,絕大多數與涉及醫療器械無明確相關性。后續監測中,尚未發現上述事件涉及醫療器械風險異常增高情況。
(三)按醫療器械管理類別統計分析
2020年,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,涉及Ⅲ類醫療器械的報告178,305份,占報告總數的33.26%;涉及Ⅱ類醫療器械的報告242,457份,占報告總數的45.23%;涉及Ⅰ類醫療器械的報告46,995份,占報告總數的8.77%;未填寫醫療器械管理類別的報告68,298份,占報告總數的12.74%。(圖7)。
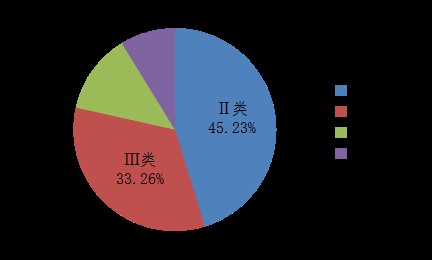
圖7 2020年醫療器械不良事件報告涉及醫療器械管理類別情況

(四)按醫療器械分類目錄統計分析
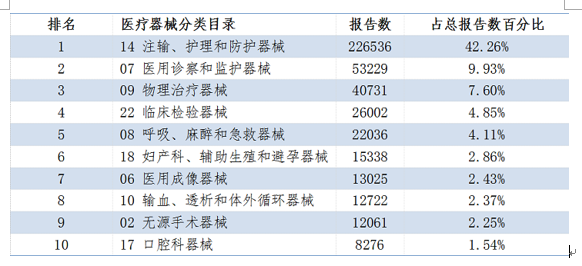
2020年,國家醫療器械不良事件監測信息系統收到的醫療器械不良事件報告涉及了醫療器械分類目錄中的所有類別。其中,報告數量排名前十位的醫療器械類別見表1。
表1 2020年醫療器械不良事件報告涉及醫療器械分類目錄情況
(五)按醫療器械結構特征統計分析
2020年,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,涉及無源醫療器械的報告345,326份,占報告總數的64.42%;涉及有源醫療器械的報告118,730份,占報告總數的22.15%;涉及體外診斷試劑的報告3,672份,占報告總數的0.69%;未填寫醫療器械結構特征的報告68,327份,占報告總數的12.75%(圖8)。
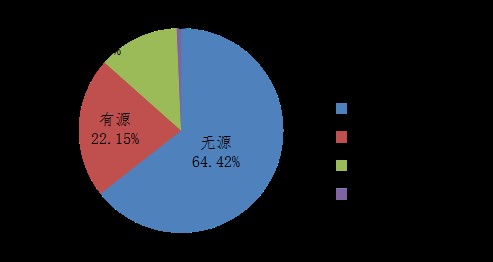
圖8 2020年醫療器械不良事件報告涉及醫療器械結構特征情況
(六)按實際使用場所統計分析
2020年,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,使用場所為“醫療機構”的報告459,553份,占報告總數的85.73%;使用場所為“家庭”的報告64,109份,占報告總數的11.96%;使用場所為“其他”的報告12,393份,占報告總數的2.31%(圖9)。
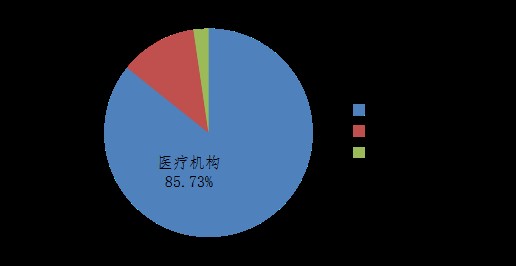
圖9 2020年醫療器械不良事件報告涉及實際使用場所情況
四、醫療器械不良事件信息通報發布情況
為及時控制醫療器械風險,對可能出現的風險提出警示,2020年,國家藥品不良反應監測中心根據日常監測中發現的風險情況,匯總相關醫療器械的主要不良事件表現,發布了1期《醫療器械不良事件信息通報》,涉及吻合器產品,向相關注冊人、使用單位等提出風險控制建議。
五、醫療器械警戒快訊發布情況
2020年,國家藥品不良反應監測中心密切跟蹤全球醫療器械監管情況,發布12期《醫療器械警戒快訊》,匯總了美國、英國、澳大利亞以及加拿大發布的包括心臟瓣膜、導尿管、監護儀、胰島素泵、呼吸機等醫療器械共79條安全性信息,為相關醫療器械在我國的安全性評價和風險控制提供參考借鑒。
六、有關情況說明
(一)與大多數國家一樣,我國醫療器械不良事件報告通過自發報告系統收集并錄入到數據庫中,即當懷疑某種事件可能與醫療器械有關時,就可以上報。受報告者主觀意識、經驗水平、認知程度、甚至所持立場等影響,醫療器械不良事件的報告可能存在片面性和局限性,如傷害程度判讀不準確、報告填寫不規范、信息不完善等,甚至將與醫療器械無關的事件也按照不良事件上報,因此統計結果與實際發生的醫療器械不良事件情況存在偏差。
(二)不同醫療器械的不良事件報告數量受使用數量、風險程度、報告意識等諸多因素影響,因此報告數量的多少不直接代表醫療器械不良事件發生率的高低或者風險嚴重程度。
(三)上述統計數據來源于國家醫療器械不良事件監測信息系統中2020年1月1日至2020年12月31日接收的數據,統計中由于四舍五入的進位規則,會出現百分比加和不等于100%的情況。
(四)本年度報告完成時,部分嚴重傷害醫療器械不良事件報告尚處在調查和評價的過程中,因此統計結果為統計時數據收集情況的真實反映,并不代表醫療器械安全性評價的最終結論。
小貼士
1.醫療器械:是指直接或者間接用于人體的儀器、設備、器具、體外診斷試劑及校準物、材料以及其他類似或者相關的物品,包括所需要的計算機軟件;其效用主要通過物理等方式獲得,不是通過藥理學、免疫學或者代謝的方式獲得,或者雖然有這些方式參與但是只起輔助作用;其目的是:
(1)疾病的診斷、預防、監護、治療或者緩解;
(2)損傷的診斷、監護、治療、緩解或者功能補償;
(3)生理結構或者生理過程的檢驗、替代、調節或者支持;
(4)生命的支持或者維持;
(5)妊娠控制;
(6)通過對來自人體的樣本進行檢查,為醫療或者診斷目的提供信息。
2.醫療器械不良事件監測:是指對醫療器械不良事件的收集、報告、調查、分析、評價和控制的過程。
3.醫療器械不良事件:是指已上市的醫療器械,在正常使用情況下發生的、導致或者可能導致人體傷害的各種有害事件。
4.死亡醫療器械不良事件報告:指患者最終結果為死亡的醫療器械不良事件報告。不表示患者的死亡與使用醫療器械有明確的關聯性。
5.醫療器械不良事件報告原則:報告醫療器械不良事件應當遵循可疑即報的原則,即懷疑某事件為醫療器械不良事件時,均可以作為醫療器械不良事件進行報告。報告內容應當真實、完整、準確。
導致或者可能導致嚴重傷害或者死亡的醫療器械不良事件應當報告;創新醫療器械在首個注冊周期內,應當報告該產品的所有醫療器械不良事件。
6.國家醫療器械不良事件監測信息系統注冊要求:注冊人、經營企業和二級以上醫療機構應當注冊為國家醫療器械不良事件監測信息系統用戶,主動維護其用戶信息,報告醫療器械不良事件。注冊人應當持續跟蹤和處理監測信息;產品注冊信息發生變化的,應當在系統中立即更新。鼓勵其他使用單位注冊為國家醫療器械不良事件監測信息系統用戶,報告醫療器械不良事件相關信息。